Практична медицина. – 2008. – № 2. – С. 204–209.
Лайм-бореліоз (ЛБ) – це природновогнищева інфекційна хвороба з групи бактеріальних зоонозів, яка передається через присмоктування кліщів і характеризується різноманіттям клінічних проявів з переважним ураженням шкіри, нервової системи, опорно-рухового апарату, серця, очей [1; 4]. ЛБ є найпоширенішою трансмісивною зоонозною інфекційною хворобою країн помірного кліматичного поясу і становить собою серйозну медичну проблему з огляду на можливість ураження багатьох органів і систем, тривалої втрати працездатності та інвалідності [5; 6; 8]. За останні роки захворюваність на ЛБ значно зросла у східноєвропейському регіоні. В Україні з її великими лісовими масивами, сформовані стійкі ендемічні ландшафтні зони зі значною концентрацією переносників хвороби – іксодових кліщів, а у прилеглих до них населених пунктах почастішали випадки захворювання.
ЛБ, як спірохетозу, притаманний цілий ряд патогенетичних і клінічних особливостей цієї групи хвороб, в тому числі здатність до тривалої персистенції збудника в організмі, поліорганність ураження, схильність до хронізації [1; 8].
Перебігу бореліозного інфекційного процесу притаманна стадійність [2; 3]. Перша стадія -– локалізований інфекційний процес на місці проникнення збудника. У 60–80 % хворих спостерігається мігруюча еритема (МЕ) в місці присмоктування кліща, яка частіше має кільцеподібну форму і вважається патогномонічним симптомом при ЛБ, а тому такі випадки хвороби не важко діагностувати. Проте при відсутності адекватної протимікробної терапії розвивається друга стадія хвороби – дисемінований інфекційний процес з ураженням багатьох органів і систем. Діагностика ЛБ може бути значно ускладнена у випадку безеритемних форм хвороби [3]. Є підстави вважати, що значна кількість безеритемних форм ЛБ не діагностується і вони перебігають під маскою багатьох неврологічних, ревматологічних та кардіологічних синдромів і хворі не отримують вчасного належного протимікробного лікування.
Метою нашої роботи було з’ясування частоти і характеру дисемінованих форм ЛБ серед пацієнтів західного регіону України.
МАТЕРІАЛИ І МЕТОДИ
Ми спостерігали 252 хворих на ЛБ. Серед пацієнтів було 90 чоловіків і 162 жінки. Середній вік 46,2±0,96 років. При первинному огляді з’ясовувалися характер провідного синдрому, важкість перебігу, а також стадія ЛБ. Наявність дисемінації інфекції підтверджувалася органними ураженнями, що свідчило про генералізацію інфекційного процесу – виявлялися вторинна еритема, гепатит, полірадикулонейропатія та інші ураження нервової системи, артрит раннього періоду, увеїт. Для специфічного підтвердження діагнозу визначали IgM і (або) IgG в ІФА. Використовувалися тест-системи «Боррелиоз-ИФА» науково-виробничої фірми «Omnix» (СПБ, Росія), “Lyme-Best” ЗАО “Vector-Best” (Новосибірськ, Росія) та “Lyme IgG ELISA” фірми “Diagnostic Automation Inc” (США).
РЕЗУЛЬТАТИ ДОСЛІДЖЕНЬ ТА ЇХ ОБГОВОРЕННЯ
Із 252 хворих на ЛБ клініко-лабораторні ознаки дисемінації хвороби виявлені у 76 хворих (30,2 %). Серед них (враховуючи поєднання різних проявів дисемінації) ураження нервової системи виявлені у 48 хворих (19,1 %), артрит – у 27 (10,7 %), гепатит – у 19 (7,5 %), вторинна еритема – у 17 (6,7 %), міокардит – у 4 (1,6 %) і увеїт – у 3 хворих (1,2 %) – мал. 1. У 16 хворих з 76 (21,1 %) патологічний процес продовжувався понад 6 міс і перейшов у хронічну фазу.
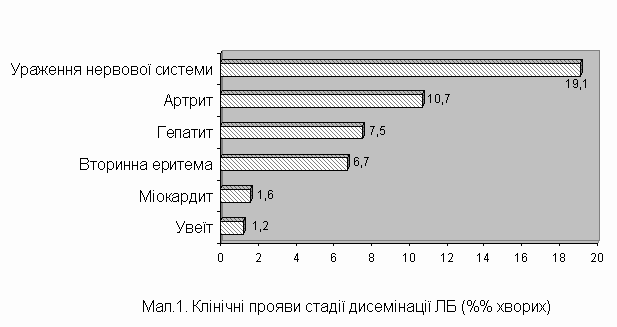
Ознаки дисемінації ЛБ були поєднаними у 28 хворих із 76 (36,8 %). Найчастіше спостерігалося поєднання уражень нервової системи з артритом – 14 хворих, або гепатитом – 6 хворих.
Із уражень нервової системи найчастіше спостерігалися полірадикулоневропатії із сенсорними і (або) моторними розладами – у 38 хворих із 252 хворих на ЛБ – 15,1 % (з них спінальна полірадикулоневропатія виявлена у 32 пацієнта і краніальна – у 6), енцефалопатія з інтелектуально-мнестичними порушеннями – у 6 (2,4 %), мононеврит – у 3 (1,2 %) і серозний менінгіт – у 2 (0,8 %) хворих. Астеновегетативний синдром без енцефалопатії спостерігався у 14 хворих (5,6 %).
Тільки у 31 пацієнтів із 48 (64,6 %), у яких виявлені неврологічні розлади, попередньо виявлялася МЕ. У решти 17 хворих спостерігалися безеритемні форми хвороби, що певною мірою ускладнювало діагностику, хоча з них 15 пацієнтів підтверджували присмоктування кліщів.
Спінальна полірадикулонейропатія супроводжувалася корінцевими болями різної інтенсивності у 15 із 32 пацієнтів, частіше в поперековому відділі, які посилювалися в нічний час. Чітка кореляція локалізації болів з місцем присмоктування кліща спостерігалася у 12 пацієнтів. У 4-х хворих болі були дуже інтенсивними, не зменшувалися після застосування нестероїдних протизапальних засобів, анальгетиків, які призначалися на догоспітальному етапі. Тільки застосування адекватної антибіотикотерапії (доксициклін, бензилпеніцилін, цефалоспорини третьої генерації) значно зменшувало больовий синдром в перші 2–3 доби і призводило до повного одужання протягом 15–20 днів. У 26 хворих із 32 (81,3 %) спостерігалися слабість і парестезії в нижніх кінцівках, а у 13 – зниження сухожилкових рефлексів. У чотирьох хворих із шести, у яких діагностована краніальна полірадикулонейропатія, виявлено парез лицевого нерва, причому у одного ураження було двобічним. У двох хворих спостерігався парез відвідного нерва, що було причиною двоїння в очах і порушення конвергенції очних яблук.
Нами обстежено 11 пацієнтів з менінгеальним синдромом з метою активного виявлення безеритемних форм нейробореліозу (НБ). Серологічне обстеження цих хворих проводилося у два етапи. Спершу визначали протибореліозні антитіла класів IgM та IgG в сироватці крові. Пацієнтам з позитивними та сумнівними результатами проводився другий етап досліджень – індикація протибореліозних антитіл паралельно в лікворі та сироватці крові з визначенням їх співвідношення – ліквор-сироваткового індексу (ЛСІ). У 2-х з 11 хворих у сироватці виявлені антитіла до борелій у концентрації, що має діагностичне значення. В обох пацієнтів у лікворі виявлені аналогічні антитіла, однак тільки в одного з них концентрація підоболонкових антитіл класу IgG була більшою, ніж у сироватці крові і ЛСІ склав 5,71 (використовувалася ІФА тест-система IDEIA Lyme Neuroborreliosis фірми “DACO”, Данія), що дозволило підтвердити діагноз НБ і призначити адекватне лікування з позитивним ефектом.
Ознаки Лайм-артриту (ЛА) виявлені у 27 з 252 хворих на ЛБ (10,7 %). З них у 18 пацієнтів попередньо спостерігалася МЕ. Встановлено, що у хворих на еритемні форми, у яких в майбутньому розвинувся ЛА, тривалість періоду від присмоктування кліща до появи еритеми становила 10,08±2,54, тоді як у всіх хворих з МЕ цей період був значно довшим – 19,27±2,51 дня (P<0,01). Це, на наш погляд, можна пояснити більшою вірулентністю та інвазивністю збудника, а відтак більшою схильністю до дисемінації з ураженням суглобів. ЛА виник через 2–3 місяці від моменту присмоктування кліща у 21 з 27 пацієнтів (77,8%), у решти 6 хворих – через 5–6 і більше місяців. Ураження суглобів характеризувалось помірними або вираженими запальними явищами у 15 пацієнтів (55,6 %), у інших пацієнтів спостерігався артральгічний варіант ураження суглобів.
У 14 хворих із 27 (51,9 %) ЛА перебігав у вигляді моноартриту (артрит колінного суглоба – у 11 пацієнтів, гомілковостопного – у 2, ліктьового – у 1), який часто асоціювався з місцем присмоктування кліща (9 хворих). У 13 хворих спостерігався поліартрит, як правило з поєднанням ураження колінних, кульшових і гомілковостопних суглобів. При артритичному варіанті ЛА у пацієнтів крім болів нами об’єктивно визначались припухлість суглобів, синовіїт. Інтенсивність запальних змін частіше помірна, ексудативний компонент незначний. Масивний синовіїт спостерігався у 2 хворих. При артральгічному варіанті пацієнтів турбували тільки болі, причому уражувалися 1–3 суглоби, переважно великі і середні. Як у випадку артритичного варіанту ЛА, так і при артральгічному варіанті основні ознаки хвороби були практично ідентичними: локалізація поблизу місця присмоктування кліща, частіше моноартрикулярний тип ураження, переважне втягнення в патологічний процес великих і середніх суглобів, міальгічний синдром, часто розвиток тендовагінітів.
Антибіотикотерапія гострих форм ЛА протягом 28 днів була високоефективною у 20 із 21 хворих (95,2 %), при хронічних формах – у 4 із 6 хворих. З огляду на те, що в патогенезі хронічних форм ЛА велику роль відіграють імунопатологічні зрушення, зокрема автоімунні явища [7], нами запропонований спосіб визначення сенсибілізації організму до антигенів борелій при ЛБ шляхом лабораторного дослідження культури лімфоцитів периферичної крові (патент на корисну модель № 26600 від 25 вересня 2007 р). Він характеризується тим, що клітинну сенсибілізацію визначають за синтезом фактору некрозу пухлин α (ФНП-α) у культурі лейкоцитів, стимульованій рекомбінантним антигеном борелій на твердій фазі. Причому, вміст ФНП-α у супернатанті визначався методом імуноферментного аналізу за допомогою комерційних тест-систем. Дослідження сенсибілізації до комплексу рекомбінантних антигенів різних геновидів борелій хворих на ЛБ (n=12) свідчило про статистично вищі показники підвищеної чутливості сповільненого типу (ПЧСТ) у хворих на хронічні форми ЛА, особливо у випадку резистентності до протимікробної терапії.
Для виявлення характеру ураження печінки при ЛБ враховувалися скарги пацієнтів (такі як погіршення апетиту, нудота, блювання, болі та важкість в правому підребер’ї). Проводилася оцінка об’єктивних даних (наявність жовтяниці, збільшення печінки), біохімічних показників сироватки крові – загальний білірубін та його фракції, аланінамінотрансфераза, тимолова проба, лужна фосфатаза. З огляду на широке поширення хвороб печінки інфекційного і неінфекційного генезу для виявлення частоти і вірогідності ураження печінки при ЛБ ми порівнювали отримані результати біохімічних тестів хворих на ЛБ з результатами аналогічних досліджень здорових донорів крові (100 чоловік), які склали контрольну групу. У 35,2 % хворих на ЛБ виявлено підвищення понад норму хоча б одного із біохімічних показників, тоді як у контрольній групі – тільки у 11 % (Р<0,001).
Клінічно виражені ознаки гепатиту виявлені у 19 із 252 хворих на ЛБ (7,5 %). Особливістю гепатиту при ЛБ був безжовтяничний перебіг з мінімальними симптомами інтоксикації і незначним підвищенням в крові рівня загального білірубіну і активності АлАТ.
Нами встановлено, що серед хворих на ЛБ інкубаційний період був суттєво коротшим у осіб з підвищеним понад норму рівнем біохімічних показників (9,18±1,58 днів), тоді як в групі хворих без ураження печінки він був значно тривалішим – 18,16±3,22 днів (Р<0,02). Частіше ураження печінки у хворих з коротшим інкубаційним періодом, як і у випадку хворих з проявами ЛА, на нашу думку, можна також пояснити більшою вірулентністю борелій, не виключено масивністю зараження і відтак вищою активністю інфекційного процесу.
Стандартна протимікробна терапія призводила до швидкої нормалізації біохімічних показників крові. При наявності у хворих ознак ранньої дисемінації збудника окрім гепатиту терміни нормалізації функції печінки були тривалішими.
Вторинна еритема виявлена у 17 хворих із 252 (6,7 %) і характеризувалася появою найчастіше 2–3 еритематозних елементів, які виникали на віддалених від місця присмоктування кліща частинах тіла і за розмірами були дещо меншими від первинної МЕ. У 12 хворих з вторинною еритемою ознаки дисемінації інфекції були поєднані, найчастіше з полірадикулонейропатією, або гепатитом.
У 11 хворих на ЛБ (4,4 %) спостерігались електрокардіографічні змінами у вигляді різного ступеня порушень провідності. У 6 хворих виявлено блокади ніжок пучка Гіса. Ще у 4-х хворих (1,6 %) спостерігалися атріовентрикулярні блокади 1–2 ступеня з мінімальними клінічними ознаками міокардиту. Електрокардіографічні зміни нормалізувалися протягом 3–4 тижнів від початку специфічної терапії. У одного пацієнта з хронічним перебігом ЛБ діагностовано міокардіопатію, яка супроводжувалася миготливою аритмією і значним зниженням скоротливої здатності серця.
У трьох пацієнтів (1,2 %) виявлено ураження органу зору у вигляді увеїту, яке виникло на другому місяці хвороби, причому у одного хворого на п’ятий день лікування доксицикліном. На нашу думку, в даному випадку руйнування борелій під дією антибіотика спричинило додаткове вивільнення мікробних ендотоксинів, що могло призвести до поглиблення морфологічних та імунопатологічних процесів і прогресуванню увеїту. Відновлення функції органа зору у всіх трьох хворих відбувалося протягом 1,5–2-х місяців.
ВИСНОВКИ
- Дисеміновані форми ЛБ можуть перебігати з ураженням нервової системи (19,1 % хворих на ЛБ), артритом (10,7 %), гепатитом (7,5 %), вторинною еритемою (6,7 %), міокардитом (1,6 %) і увеїтом (1,2 % хворих).
- Для попередження дисемінації інфекції і розвитку органних уражень у хворих на безеритемні форми ЛБ важливою є вчасна діагностика і адекватна протимікробна терапія, для чого хворим з відповідною клінічною симптоматикою за наявності анамнестичних даних про присмоктування кліщів необхідно проводити специфічні серологічні дослідження.
ВИКОРИСТАНА ЛІТЕРАТУРА
- Воробьева Н.Н. Иксодовые клещевые боррелиозы // Рос. мед. журн. – 2000. – № 6. – С. 33–38.
- Лесняк О.М., Беликов Е.С. О классификации Лайм-боррелиоза // Терапевт. арх. – 1995. – Т. 67, № 11. – С. 49-51.
- Лобзин Ю.В., Усков А.Н., Антонов В.С. и др. Клиника и лабораторная диагностика Лайм-боррелиоза // Учен. зап. Санкт-Петербург. гос. мед. ун-та им. Павлова. – 2000. – Т. 7, № 1. – С. 15–22.
- Малый В.П., Кратенко И.С. Системный клещевой боррелиоз. – 2006. – 128 с.
- Савчак В.І., Андрейчин Ю.М. Хвороба Лайма (бореліоз) // Лікарська справа. – 1998. – С. 134–136.
- Melski J.W. Lyme borreliosis // Semin. Cutan. Med. Surg. – 2000. – V. 19, N 1. – P. 10–18.
- Sibilia J., Jaulhac B., Limbach F.X. Rheumatologic manifestations of Lyme borreliosis // Rev. Med. Interne. – 2002. – V. 23, N 4. – P. 378–385.
- Steere A.C. Lyme Disease // N. Engl. J. Med. – 2001. – V. 345. – P. 115–125.
О.М. Зінчук
ОСОБЛИВОСТІ КЛІНІКИ ТА ДІАГНОСТИКИ ДИСЕМІНОВАНИХ ФОРМ ЛАЙМ-БОРЕЛІОЗУ
У статті висвітлено клінічні особливості дисемінованих форм Лайм-бореліозу. Встановлено, що у 30,2 % хворих на Лайм-бореліоз визначаються клінічні і лабораторні ознаки дисемінації збудника. Лайм-бореліоз – ендемічна інфекційна хвороба з трансмісивним шляхом передачі, яка часто має хронічний, рецидивуючий перебіг з поліорганними ураженнями. Хвороба широко поширена в середній смузі північної півкулі, реєструється у теплу пору року відповідно до біології переносника і характеризується у більшості випадків наявністю мігруючої еритеми на місці присмоктування кліща, явищами інтоксикації, а також схильністю до хронізації з ураженнями центральної і периферичної нервової системи, опорно-рухового апарату, серця, очей.
Ключові слова: хвороба Лайма, борелії, бореліоз, кліщі, нейропатія, артрит, гепатит, увеїт.
O.M. Zinchuk
CLINICAL AND DIAGNOSTIC FEATURES OF DISSEMINATED FORMS LYME DISEASE
The article describes investigations results on frequency and character of disseminated forms Lyme disease. It is established that 30,2 % of patients have disseminated Lyme disease. Lyme disease is wide-distributed vernacular spirochetosis with vector-borne transmission pass, which often has long-lasting relapsing course of disease with polyorganic involvement. Lyme disease is characterized by the presence of erythema migrans in the site of inoculation, chronization in the follow-up period with involvement of central and peripheral nervous system, joints, heart, and eyes.
Keywords: Lyme disease, borrelia, borreliosis, ticks, neuropathy, arthritis, hepatitis, uveitis.


